
복잡한 국내외 규제(MFDS, FDA 등)는 저희에게 맡기고, 개발에만 집중하세요.
초기 단계부터 걱정 없이 성공적인 사이버보안 관련 승인을 보장합니다.
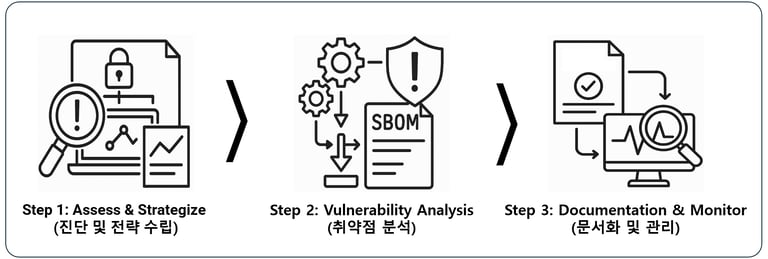
SECURIMD의 단계별 프로세스

혹시 시험을 완료했더라도 걱정 마세요. 현 단계에 딱 맞는 최적의 솔루션으로 사이버보안 승인을 빠르게 지원해 드립니다.
Step 1: Assess & Strategize — 진단 및 전략 수립
귀사의 제품·개발 프로세스 전반을 분석해 규제·보안 리스크를 도출하고, 우선순위에 따른 맞춤형 대응 로드맵을 수립합니다.
- 자산 식별 (데이터 및 기술 자산)
- 위협 모델링
- 규격 또는 가이드라인 기준 격차 분석
Step 2: Vulnerability Analysis — 취약점 분석
제품 소프트웨어·펌웨어·네트워크 연결부 및 공급망 요소에 대해 정적·동적·구성 검토를 수행해 실질적 취약점을 발굴하고 재현시험을 통해 영향도를 평가합니다.
- SBOM 기반 취약점 분석
- 시큐어 코드 스캔 (SAST)
- 펌웨어/하드웨어 보안 검토
- 모의 침투
Step 3: Documentation & Monitor — 문서화 및 지속 관리 (1년)
승인 제출에 필요한 기술·보안 문서를 완성하고, 제품 출시 이후엔 모니터링·취약점 대응 체계를 지원하여 규제 변경이나 신규 위협에 신속히 대응합니다.
- 규제 제출용 보안문서 작성 (사전/사후)
- 보안 업데이트 프로세스 지원
- SBOM 관리


SECURIMD의 차별화된 가치
첫째, 일반 IT가 아닌, 의료기기 특화 전문가: 임상 환경과 소프트웨어 특성을 깊이 이해하는 의료기기 전문 사이버보안팀이 제품 라이프사이클 전반에 걸쳐 현실적이고 실행 가능한 맞춤형 솔루션을 제공합니다.
둘째, FDA/EU MDR/디지털의료제품 등 규제 승인 가속화: FDA, EU MDR, 국내 규제에 대한 풍부한 사이버보안 실무 경험을 바탕으로, SDLC, SBOM 등 최신 요구사항에 완벽히 대응합니다. 복잡한 인허가 절차 및 심사 과정의 보완에도 신속히 대응하여 제품의 빠른 승인을 보장합니다.
셋째, 시간과 비용을 아끼는 원스톱 통합 서비스: 설계 자문, 문서 준비, 기술 테스트까지 모든 사이버보안 요구사항을 한 곳에서 해결합니다. 여러 업체를 관리할 필요 없이 일관된 전략을 통해 시간과 비용을 절약하고, 고객사는 핵심 제품 개발에만 집중할 수 있습니다.
넷째, 최신 사이버보안 솔루션: FDA 권고사항, IEC 62443, 전자적 침해행위 보안지침 등의 표준 또는 가이드라인에 기반한 컨설팅과 테스트를 제공합니다. 최신 사이버 위협 동향을 지속적으로 반영하여 평가 기법을 업데이트하며, 고객 제품이 최신의 규제 준수 상태를 유지하도록 지원합니다.
다섯째, 제품 출시 후에도 지속되는 신뢰 파트너십: 단순한 일회성 서비스가 아닌, 출시 후에도 보안 상담, 문서 업데이트, 교육 등 지속적인 지원을 제공합니다. 최상의 결과로 매 프로젝트마다 신뢰를 구축하며, 고객사의 장기적인 보안 안정성을 보장합니다.

